南方医学网讯:近日,浙江大学化学系邬建敏课题组在ACS Nano上发表了基于组织转印技术的质谱成像新方法,实现了TCSI-MS在组织分子成像领域的应用。
背景介绍
分子病理作为跨界融合的技术逐渐成为精准医疗的支柱,其在疾病的鉴别诊断、伴随诊断、分子分型、预后判断等方面起到极其重要的作用。目前,分子病理学中常用的技术包括高通量基因测序(NGS),荧光原位杂交(FISH),免疫组化(IHC)、基因芯片及PCR技术等。随着精准医学的发展,对复杂疾病尤其是恶性肿瘤等疾病的个性化精准治疗需要从更多维度的分子角度对病理组织样本进行分型和判别。由于质谱技术的高通量,免标记特点,质谱成像、质谱组织活检、流式细胞质谱等技术将成为分子病理领域的重要方向。
脂质与细胞增殖、细胞物质交换与能量交换、细胞信号传导等重要生理生化过程密切相关。基于空间脂质组学的分子病理研究对于推动精准医学的发展具有重要意义。质谱成像是空间脂质组学的主要解决方案。其中,基质辅助激光解吸离子化质谱成像( MALDI-MSI)是应用最为广泛的质谱成像技术,但由于有机小分子基质的背景干扰、结晶不均匀性及前处理时间长等缺点使得常规MALDI-MSI在临床应用中受到阻碍。化学系邬建敏课题组此前在免基质脂质分析领域开展了一系列的研究。该课题组利用垂直硅纳米线(SiNW)顶端的电磁增强效应,提出了顶端接触取样原位离子化质谱技术(TCSI-MS),实现了组织样本脂质分子的快速获取(ACS Appl. Mater. Interfaces,2018,10, 14389).与附属邵逸夫医院合作成功地将TCSI-MS技术应用于肝癌组织样本的良恶性判断和切缘判别 (Anal. Chem. 2019,91, 10376)。TCSI-MS技术通过组织与纳米线顶端的接触,将组织脂质分子转印到纳米线,在后续的质谱分析中,激光轰击纳米线顶端进而实现组织样本分子的无损分析。该方法支持同一个组织样本的跨平台分析,便于获取多组学分子信号。然而,因硅纳米线阵列表面的空间不均匀性,TCSI-MS在组织成像、空间代谢组或脂质组学的应用仍然面临挑战。发展一种能高保真呈现脂质分子在组织表面空间分布的免标记成像基板是解决TCSI-MS在分子病理领域应用的关键。
近日,化学系邬建敏课题组在ACS Nano上发表了基于组织转印技术的质谱成像新方法,实现了TCSI-MS在组织分子成像领域的应用。
工作亮点
研究人员首先使用自下而上生长的两亲性氮掺杂石墨烯量子点(NGQD)作为插层剂和分散剂来辅助MoS2的液相剥离,以获得薄而稳定的NGQD@MoS2二维纳米片。然后通过自组装过程将它们负载到硅纳米线(SiNWs)的顶端,获得一种新型的NGQD@MoS2/SiNWs质谱成像基板(图1)。
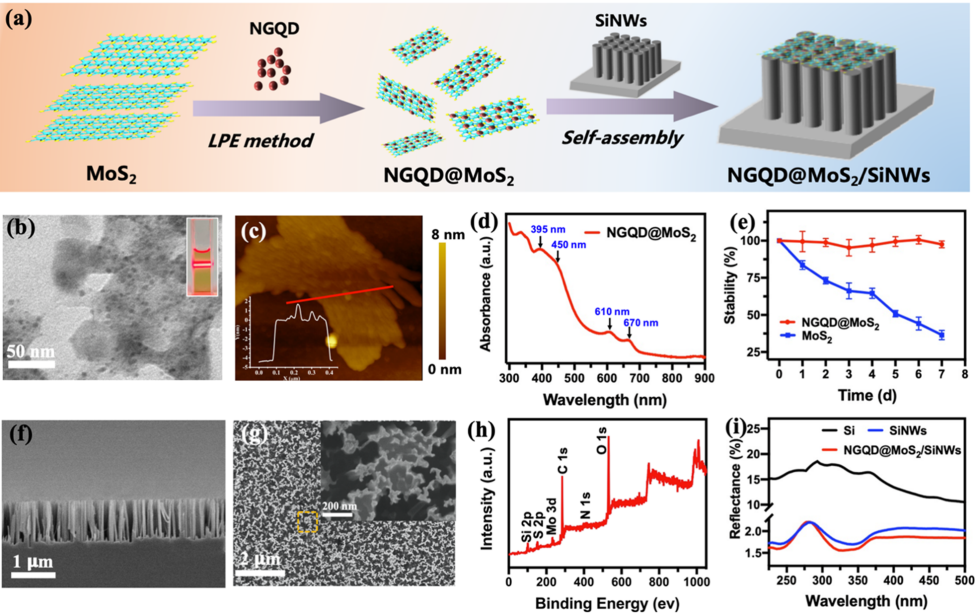
图 1. (a)NGQD@MoS2/SiNW基板合成流程示意图;(b)NGQD@MoS2纳米片TEM图像;(c)NGQD@MoS2纳米片AFM图像;(d)NGQD@MoS2纳米片紫外吸收曲线;(e)NGQD@MoS2与MoS2纳米片稳定性比较;(f)NGQD@MoS2/SiNW截面SEM图像;(g)NGQD@MoS2/SiNWs表面 SEM图像;(h)NGQD@MoS2/SiNW XPS谱图;(i)Si,SiNWs, NGQD@MoS2/SiNWs紫外漫反射曲线。
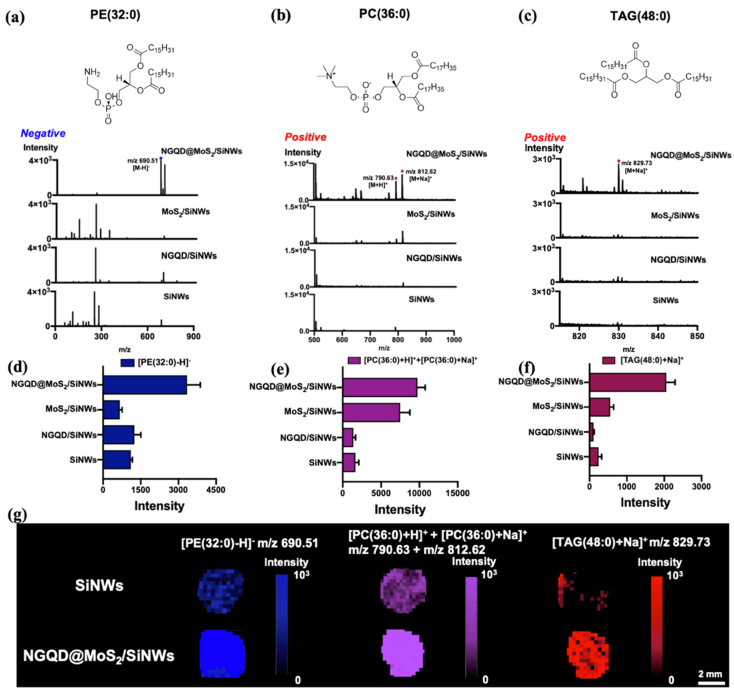

图 3.(a)靛蓝分子在负离子模式下的谱图;(b)-(c)靛蓝分子总离子强度对比图;(d)协同机理示意图;(e)苄基吡啶盐正离子模式谱图;(f)苄基吡啶盐总离子强度对比图;(g)存活率曲线。
得益于NGQD@MoS2/SiNWs基板的高LDI效率和优异的分子成像能力,研究人员成功地对小鼠肺组织进行了印迹质谱成像。在NGQD@MoS2/SiNWs上获得的脂质数量和总离子强度比在 SiNWs基板上高 4-5倍。成像结果可清晰显示小鼠肺组织的脂质分子空间分布和空泡孔洞结构(图 4)。此基板可兼容印迹采样和成像的功能,具有抗干扰能力强、灵敏度高等优点。该方法将质谱成像前处理流程缩短至10分钟以内,更有利于与临床医学研究相结合。
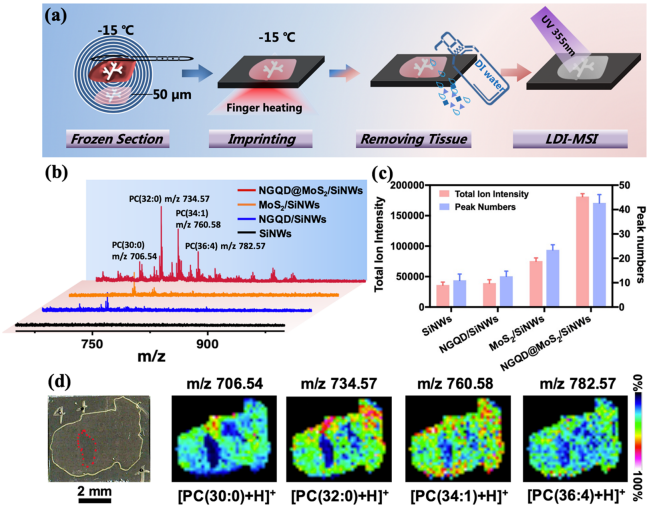
图4. (a)印迹质谱成像流程;(b-c)不同基板获得的成像效果对比;(c)小鼠肺组织质谱成像图。

原文链接:
https://pubs.acs.org/doi/full/10.1021/acsnano.2c02616