胆管癌(CCA)由一组高度侵袭性和异质性的胆道恶性肿瘤组成。由于其恶性程度高、初始症状较弱、易复发和转移,因此死亡率高。通常,成像技术(超声、计算机断层扫描、磁共振成像/磁共振胰胆管造影、正电子发射断层扫描)的敏感性有限。因而在检测CCA时,必须辅以组织活检来确诊。目前可用的血清生物标志物,如碳水化合物抗原19-9(CA19-9),由于其敏感性和特异性较低,在CCA的诊断中并不可靠。因此,大多数CCA患者通常在癌症处于晚期时被诊断出来,由于该阶段的治疗选择很少,导致死亡率增加。长期胆道炎症或结石是CCA的高危因素,这些良性胆道疾病患者(BBD)通常具有高CA19-9,难以与CCA区分开来。因此,迫切需要具有高敏感性和特异性的非侵入性生物标志物来准确诊断BBD和恶性CCA患者。
脂质分子是细胞膜的关键组分,参与多种重要的生命活动,多肽含有丰富的疾病特异性信息,因而,脂质和多肽已成为临床研究中许多疾病的候选生物标志物。脂质组学和多肽组学在挖掘HCC和CCA诊断标志物方面的作用也被研究证实。现阶段,脂质组学和多肽组学多采用胆汁样本对CCA诊断,这是因为其位置接近胆管,可以增加发现CCA特异性生物标志物的可能性。然而,胆汁采集是侵入性的,很难从各个CCA阶段的患者身上获得。血清作为反映患者全身代谢失调的代谢库,取样创伤小与胆汁相比,血清更容易用于临床诊断。然而目前对CCA血清脂质组学和多肽组学的研究较少。从系统生物学的角度来看,多组学数据的互补和整合分析将全面揭示疾病状态,阐明疾病机制,从而提高诊断的准确性。因此, CCA血清多组学研究具有较好的价值潜力,有望满足临床对CCA诊断的需求。
近日,浙江大学化学系邬建敏教授带领的纳米医学与创新诊断技术联合实验室在美国化学会著名期刊Journal of Proteome Research上发表了题为 “Accurate Discrimination of Benign Biliary Diseases and Cholangiocarcinoma with Serum Multiomics Revealed by High-Throughput Nanoassisted Laser Desorption Ionization Mass Spectrometry”的论文。该实验室发展了高通量纳米辅助激光解吸电离质谱(NALDI-MS)技术,并通过揭示BBD和CCA患者血清脂质和多肽分子的扰动,实现了BBD和CCA的精准诊断(图1)。此外,转录组学的整合,进一步揭示了脂质和多肽在CCA进展中的作用。
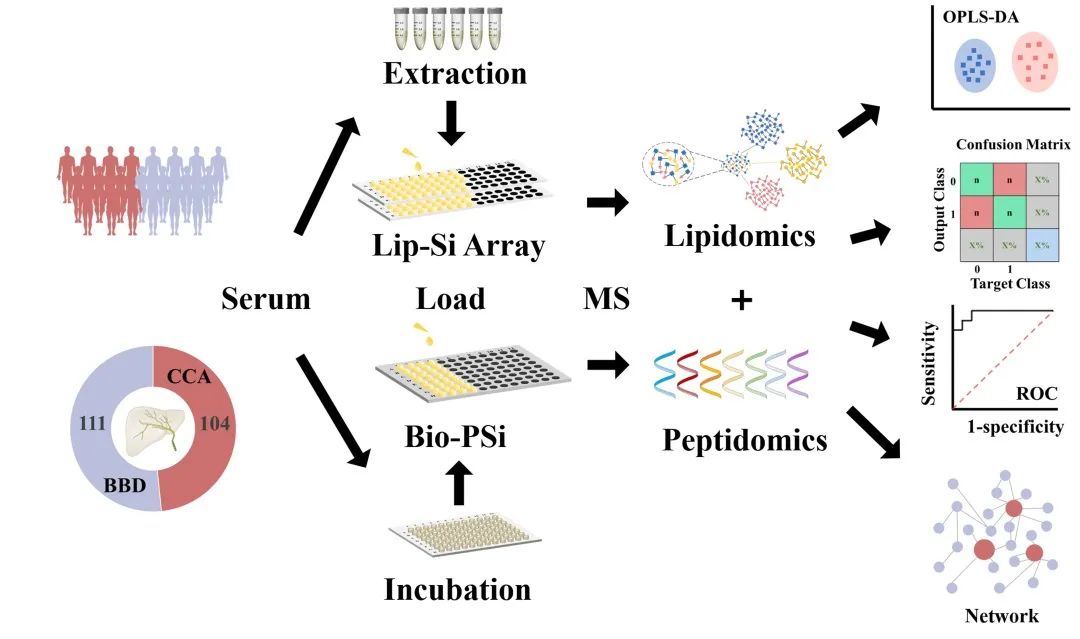
图1 基于NALDI-MS技术的良性胆道疾病和胆管癌患者血清脂质组学和多肽组学分析工作流程。
该工作采用Lip-Si Array®微纳质谱芯片和Bio-pSi®血清多肽检测试剂盒(汇健科技提供)分别进行脂质谱和多肽谱的检测。基于Lip-Si Array®芯片可实现血清中482个有效脂质峰(S/N≥5)的检测,批次间的中位RSD值为15.7%。Bio-pSi®试剂盒中的微纳颗粒材料可有效排除大分子蛋白质,并选择性富集分子量小于20 KDa的血清多肽,检测血清多肽的质谱出峰强度和覆盖度均优于常规磁珠,批间CV可控制在15%以内,基于汇健科技微纳材料技术和临床质谱技术的血清双组学通量高、稳定性高。
该技术在临床的诊断判别中表现出巨大的潜力。实验室联合浙大附属邵逸夫医院肝胆专家蒋智军主任开展了BBD和CCA的血清多组学诊断研究。本项研究共纳入123例BBD患者和112例CCA患者。血清脂质组学和多肽组学的统计分析分别筛选出P<0.05的93个差异脂质峰和81个差异多肽峰。两种组学的监督聚类热图均清楚地显示了BBD和CCA组之间的不同(图2A,B)。基于P <0.05和OPLS-DA中VIP >1的条件共筛选出20种特征脂质和5种特征多肽。可以看到基于特征脂质或者多肽的OPLS-DA分析只能部分区分BBD和CCA组(图2C,D)。但如果整合20种脂质和5种多肽后,则可以实现BBD和CCA组的明确区分(图2E)。
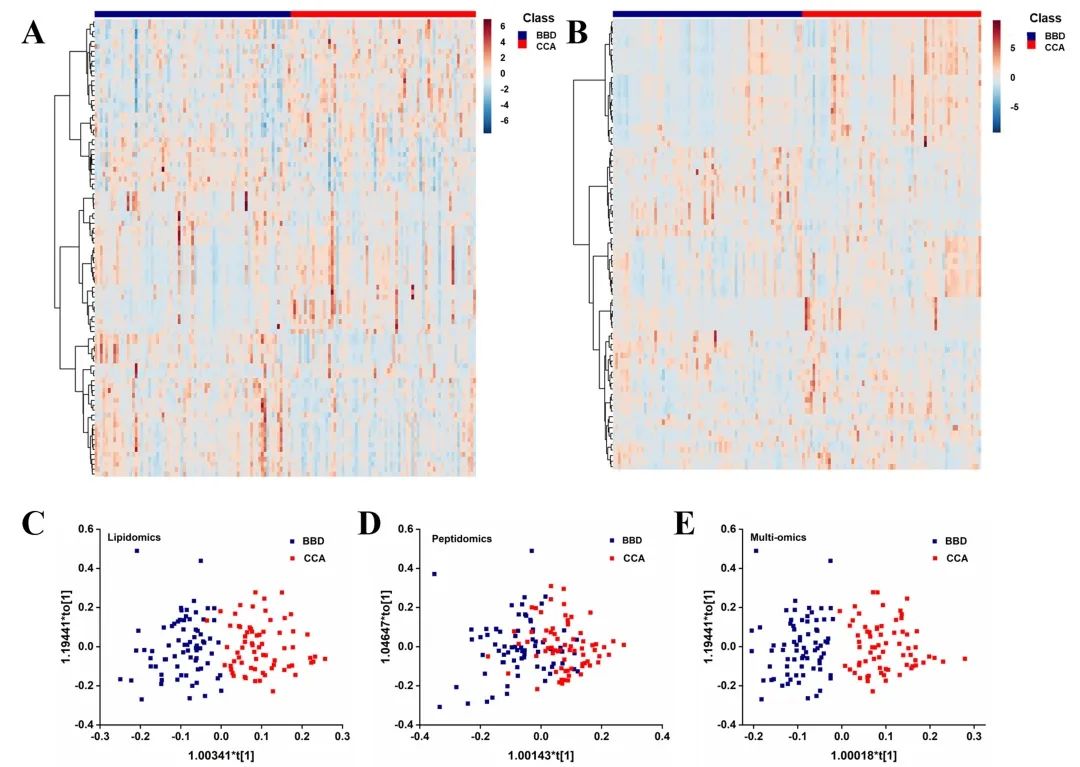
图2 BBD和CCA患者的血清脂质组学和多肽组学分析。BBD和CCA组中(A)差异脂质峰(P<0.05)和(B)差异多肽峰(P<0.05)的聚类热图。基于BBD和CCA组中(C)特征脂质、(D)多肽组学和(E)多组学的OPLS-DA图。
选用三种不同类型的机器学习算法(ANN、LASSO、SVM)评估了脂质组学、多肽组学和多组学模型在CCA诊断中的性能,结果表明由ANN算法构建的多组学模型显示出最佳诊断性能,敏感性和特异性分别为96.5%和96.4%(图3A)。ROC曲线显示多组学模型的诊断能力远高于临床常用CCA肿瘤标志物CA19-9(图3B)。值得注意的是,基于ANN构建的多组学模型可以指示CCA早晚期的进展(图3C)。此外,外部测试队列中良好的诊断结果证实了该模型的泛化能力(图3D)。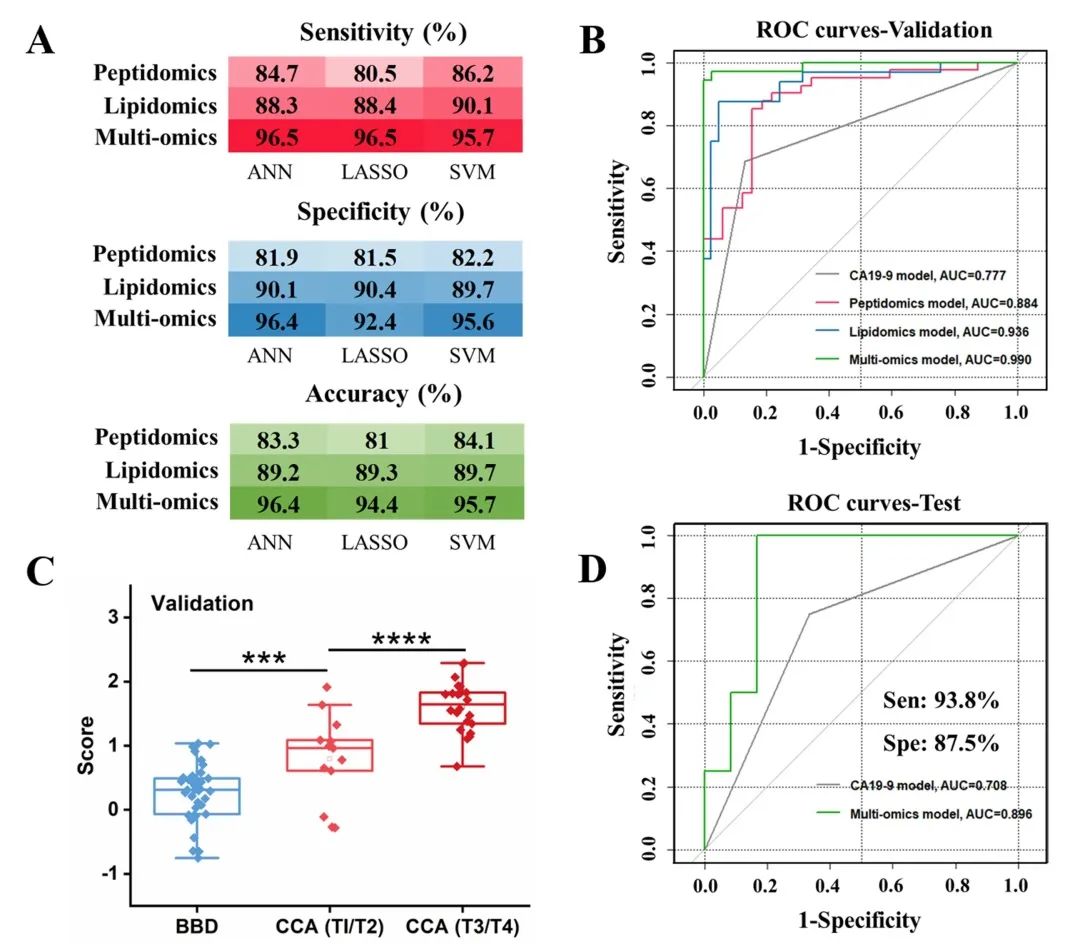
图 3 基于机器学习算法的CCA潜在生物标志物验证。(A)验证组中基于不同机器学习算法的诊断模型的敏感性、特异性和准确性。(B)验证组中不同诊断模型的ROC曲线。(C)验证组中BBD患者和不同阶段的CCA患者的多组学模型综合得分的箱线图。***:P<0.001;****:P<0.0001。(D)测试组中不同诊断模型的ROC曲线。
TCGA中转录组学数据的进一步整合揭示了 CCA 进程中鞘脂、甘油酯、甘油磷脂和蛋白质-脂质复合物的明显扰动。这一结果也与研究中脂质组学和多肽组学结果一致。此外,75个基因的PPI 网络分析显示扰动的基因主要在脂质转运和脂蛋白复合物重塑中发挥重要作用(图4),进一步从基因层面证明CCA进展中脂质和多肽的扰动。
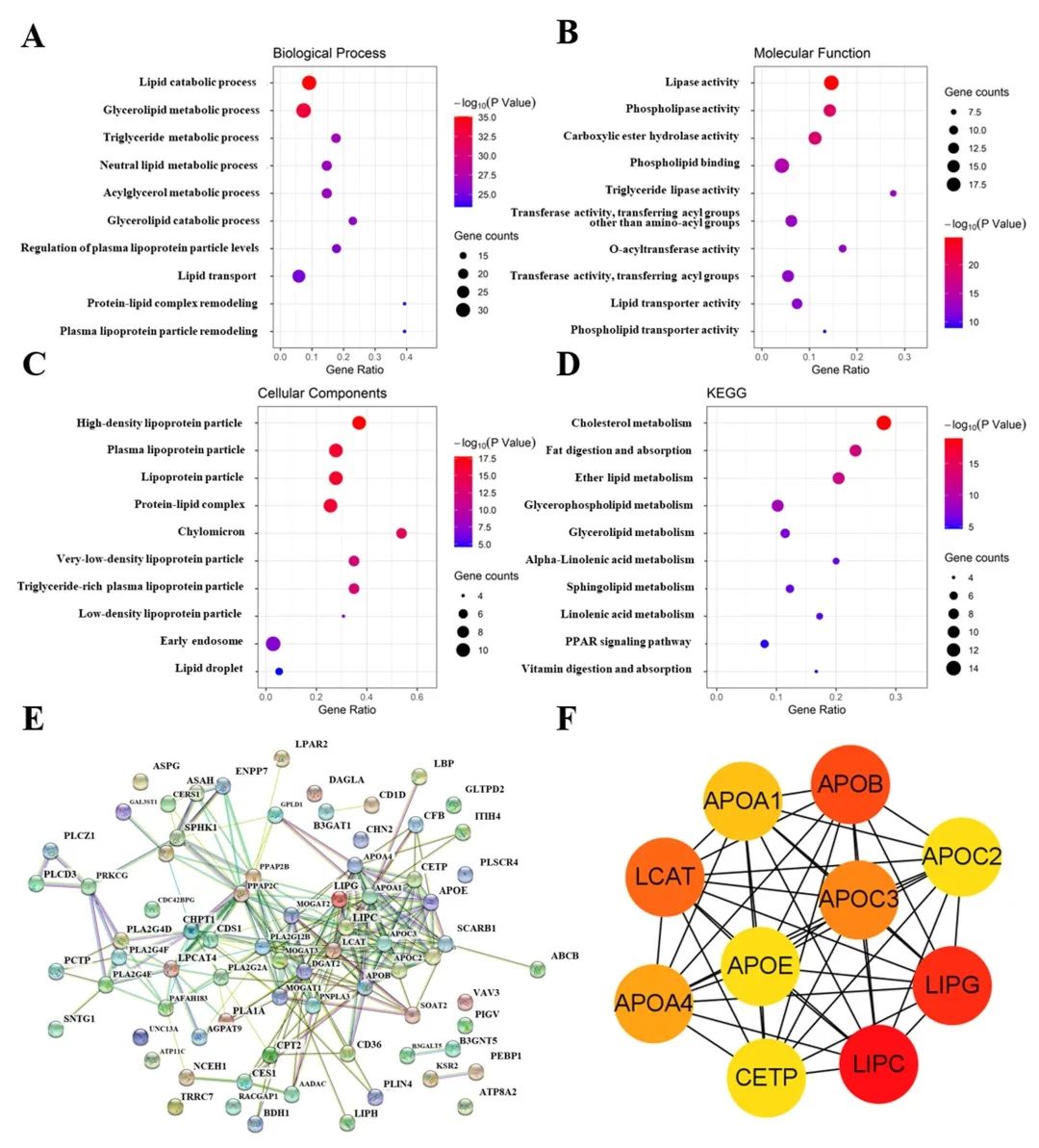
图 4. 整合基因的功能富集分析和PPI网络分析。(A)生物过程分析。(B)分子功能。(C)细胞成分分析。(D)KEGG通路分析。(E)整合基因的PPI网络。(F)PPI网络中前10个枢纽基因的连接。
此项工作的第一作者是浙大化学系2019级直博生曲雪彤。研究工作受到国家自然科学基金(No.21874118)、浙江省自然科学基金(No.LQ21H160031)、浙江省重点研发计划(No.2021C03127)、浙江省重大医学科技计划(No. WKJ-ZJ-2030)和杭州汇健科技有限公司的资助。
杭州汇健科技有限公司(以下简称“汇健科技”)成立于2016年11月,是一家集体外诊断、医学检验、个人健康监测为一体的国家高新技术企业。汇健科技通过先进的半导体纳米技术和人工智能算法,建立了高通量临床质谱及人工嗅觉传感两大技术平台;运用纳米材料技术(MT)、高通量生 物检测技术(BT)、数据库及AI算法(IT),构建了基于“3T"的多组学多元样本诊断及健康监测产品及服务平台,有力赋能组学技术在液体活检、组织活检及呼气筛查中的应用。
汇健科技与国内外顶尖学术机构、医疗机构、产业链合作伙伴开展多个领域的密切合作,积极推动创新组学技术在医学领域的科学研究、临床实践及应用转化。其产品与服务将广泛应用于肿瘤筛查、辅助诊断、预后判断、用药指导、手术指导、疗效监测以及慢病管理等多个临床场景。公司以感知-汇知-智慧为理念,打造技术驱动型医疗科创企业、服务全球医疗健康事业。